
发布时间: 2026-03-29 18:22:57
1、导读
膝骨关节炎(KOA)不仅会带来长期的肌肉骨骼疼痛负担,还常伴随轻度认知障碍(MCI)等神经认知功能异常,而慢性低度炎症被认为是两者共病的关键介导因素。尽管目前已有研究发现促炎细胞因子可穿透血脑屏障并与大脑默认模式网络异常有关,但KOA相关炎症信号如何导致MCI相关大脑区域功能改变的神经生物学具体路径仍未被完全阐明。此外,既往文献较少系统性地探讨KOA特异性炎症特征是否优先影响MCI相关的大脑网络,本研究从这一亟待完善的角度出发,深入探讨了炎症介导下脑功能重组规律及其作为早期预测标志物的潜力。
2025年9月,湖北文理学院附属襄阳市中心医院Zhengxi Li教授团队在《Arthritis Research & Therapy》发表了一项整合神经影像学、炎症生物标志物和机器学习的观察性研究。结果显示,MCI相关的大脑功能改变主要集中在内侧前额叶皮层(mPFC)、楔前叶和颞上回,且mPFC的局部一致性(ReHo)显著介导了外周IL-6升高与认知衰退的关系。作者得出结论,IL-6驱动的mPFC功能障碍是连接KOA相关炎症与MCI的潜在神经途径,结合这些区域的ReHo/ALFF指标可作为早期检测认知脆弱性的可靠生物标志物。
2、研究方法
本研究采用了一项整合临床数据、静息态功能核磁共振(rs-fMRI)以及机器学习的横断面观察性研究设计。在人群入排标准方面,主要纳入符合美国风湿病学会(ACR)标准、Kellgren-Lawrence分级≥II级、年龄在50-65岁的右利手KOA患者,并排除了合并其他炎症性关节炎、严重全身性疾病或神经精神疾病的患者。研究将入组受试者划分为健康对照组(HC)、伴有MCI的KOA组(KOA-MCI)以及不伴有MCI的KOA组(KOA-non-MCI),通过采集外周血经离心及ELISA试剂盒检测获取连续型变量(促炎细胞因子IL-6和TNF-α的血清浓度),并进行了头颅fMRI扫描。结局指标主要包括蒙特利尔认知评估量表(MoCA)得分(总分低于26分定义为认知能力受损),以及基于fMRI数据经过时间校正、空间标准化、平滑滤波等预处理后计算得出的体素水平局部一致性(ReHo)和低频波动振幅(ALFF)数值。
在统计与分析方法上,主要结局指标ReHo和ALFF的体素级差异是通过单因素方差分析(ANOVA)进行处理的,模型中将年龄、性别和教育年限作为协变量以控制混杂因素,随后采用事后两样本T检验分析组间差异。为探究变量间的潜在因果链条,作者采用Bootstrapping中介分析算法(PROCESS宏)来评估特定脑区的ALFF/ReHo特征在炎症细胞因子水平与MoCA得分之间是否存在间接中介效应。此外,研究提取具有中介效应的脑区功能指标作为特征,采用线性判别分析、梯度提升、AdaBoost等多种机器学习算法构建模型并在外部独立队列中进行测试,旨在验证特定网络异常特征在预测疾病认知状态中的临床普适性与转化价值。
3、研究结果
人口统计学特征
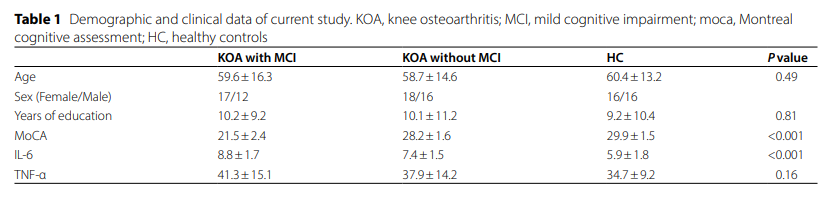
三组人群(健康对照组、KOA伴MCI组、KOA不伴MCI组)在年龄、性别构成比和受教育年限方面均未观察到具有统计学意义的显著差异(P值均>0.05)。这表明该研究队列中各组患者的基线人口学特征匹配良好,排除了这些基础因素对后续脑功能和认知评估结果的干扰(表1)。
临床与炎症评估
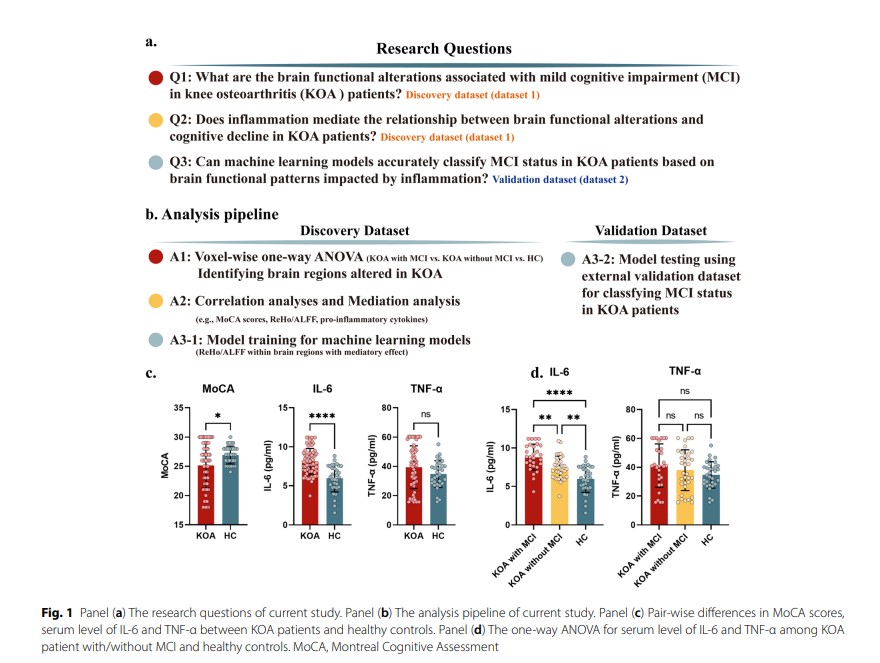
KOA伴MCI患者的MoCA评分显著低于对照组,同时其血清IL-6水平(8.8±1.7 pg/ml)显著高于KOA不伴MCI组和健康对照组(P<0.01)。该结果证实了外周退行性关节疾病确实伴随认知功能受损风险,且显著升高的特异性促炎细胞因子IL-6构成了认知衰退进程中的关键病理特征(表1、图1.c、图1.d)。
ReHo与ALFF分析
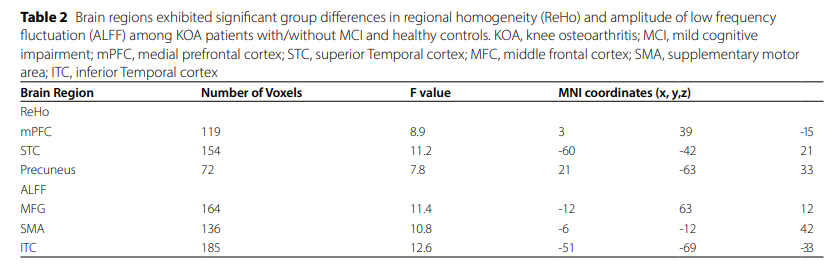
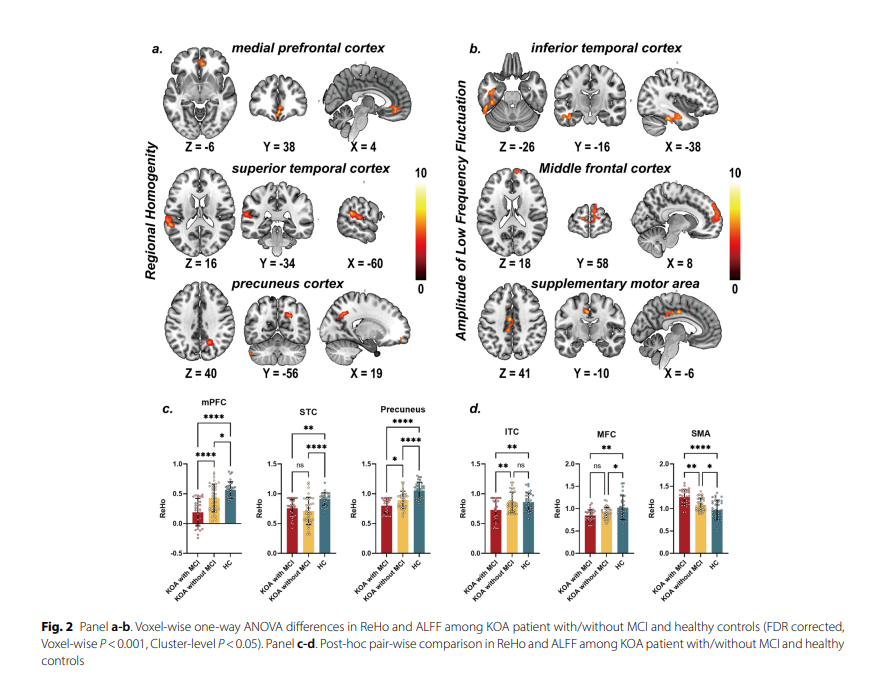
组间神经影像对比显示,KOA伴MCI患者在内侧前额叶皮层(mPFC)的ReHo发生显著改变(F=8.9,聚类水平P<0.05),而在辅助运动区(SMA)和颞下皮层的ALFF也存在显著的组间差异。这提示合并轻度认知障碍的膝骨关节炎患者,在其大脑默认模式网络核心枢纽及感觉运动区域内,已经出现了特异性的局部神经活动与功能连接的病理性重组(表2、图2)。
中介效应分析
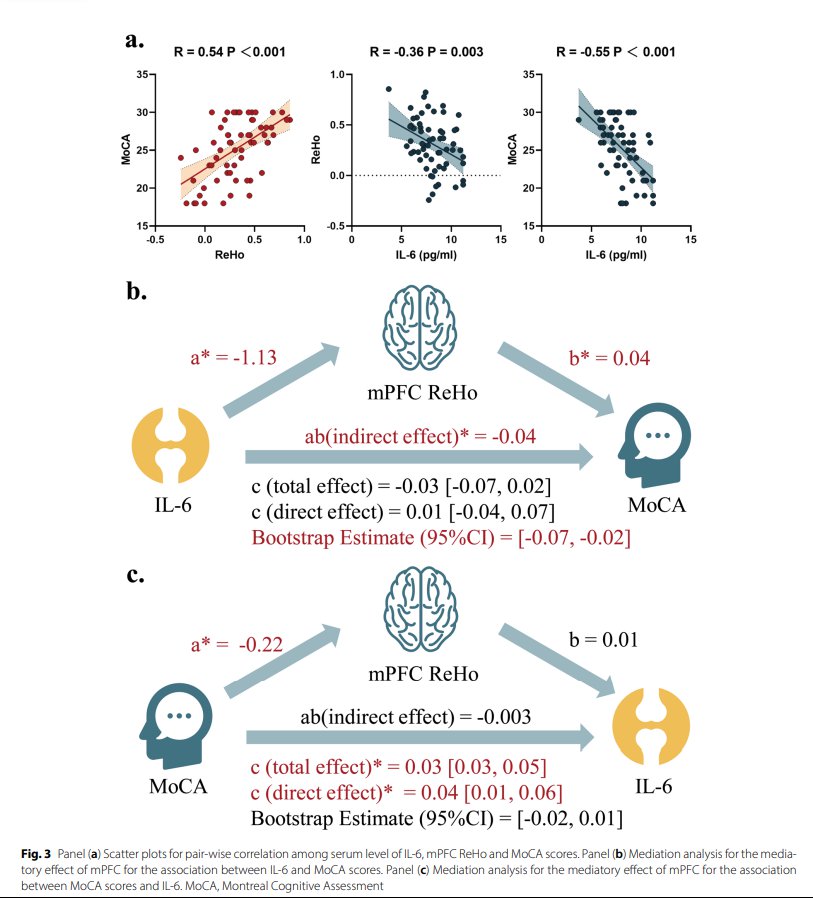
相关与中介模型揭示,mPFC区域的ReHo与MoCA得分呈显著正相关(R=0.54,P<0.001),与IL-6水平呈负相关(R=-0.36),且mPFC ReHo在IL-6水平抑制认知得分的路径中发挥了显著的间接中介作用(间接效应ab=-0.04)。由此可推断,外周升高的IL-6炎症信号是通过削弱和破坏mPFC脑区的局部神经功能一致性这一桥梁,实质性地参与并促发了KOA患者的认知能力衰退(图3)。
机器学习分类验证
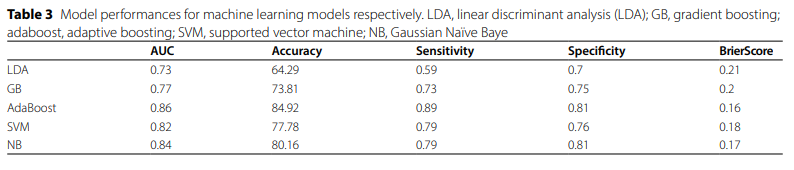
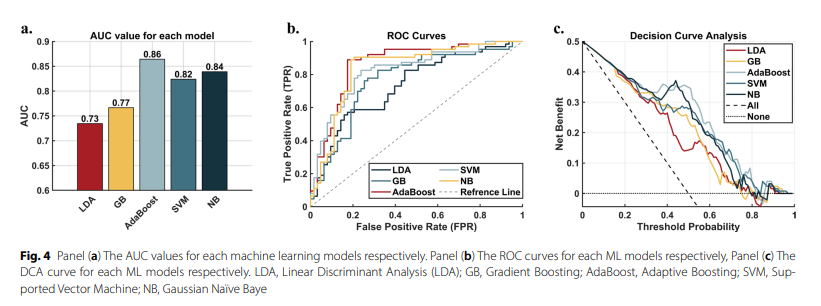
在独立的外部验证集中,以mPFC ReHo值为特征训练的AdaBoost机器学习分类模型展现出最优异的预测效能,其受试者工作特征曲线下面积(AUC)高达0.86,分类准确率为84.92%。这一优异表现强有力地确证了:提取受炎症驱动的mPFC功能重组特征作为神经影像生物标志物,在早期辅助鉴别和预测KOA人群MCI发生风险方面具有极高的临床应用潜力(表3、图4)。
4、舟舟点评
研究前证据:既往的流行病学证据已经充分揭示了膝骨关节炎(KOA)与阿尔茨海默病等神经退行性疾病风险增加之间的密切重叠。基础科学与部分影像学研究也指出,伴随关节退变而产生的慢性系统性低度炎症(尤其是循环中升高的IL-6和TNF-α)是导致“炎症衰老”和神经元突触重塑受损的潜在桥梁,且可能引发默认模式网络(DMN)的功能异常。
研究附加值:本研究的核心附加值在于成功闭环了“外周炎症靶点-中枢网络异常-宏观认知受损”的证据链。研究团队不仅精准识别了内侧前额叶皮层(mPFC)和楔前叶等区域在病程中的特异性改变,更通过严格的中介效应分析,首次确证了“IL-6驱动的mPFC局部一致性(ReHo)降低”是触发KOA相关MCI的核心机制路径。此外,利用多中心数据验证机器学习模型预测能力的创新设计,极大地提升了该影像学发现的鲁棒性和转化为临床检测工具的可行性。
对现有证据的影响:本研究结果对未来老龄化疾病的管理政策和临床实践具有深远的指导意义。它提示临床在制定KOA的标准护理流程时,有必要前瞻性地纳入血液炎症标志物筛查与早期认知状态评估。更重要的是,本研究为未来的干预性试验锚定了明确的方向:针对IL-6炎症通路的靶向抗炎干预、结合生活方式调整或更积极的疼痛管理,极有可能成为逆转或延缓骨关节炎人群神经功能衰退、提升整体生命质量的有效前沿干预策略。

下一篇:非整倍体四联征以100%特异性预测早期流产染色体异常